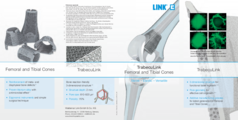
Cônes fémoraux et tibiaux TrabecuLink

Visit also our FlexiCone Microsite - click here!
- Stabilité – avec fixation non cimentée
- Élasticité – grâce aux axes de flexion intégrés
- Adaptabilité – pour une large gamme de solutions7
Les cônes fémoraux et tibiaux dynamiques TrabecuLink offrent une solution intéressante pour assurer la restauration non cimentée de défects osseux10 et fournir un support supplémentaire à la prothèse en cas de perte de substance osseuse dans le tibia proximal. La conception dynamique5,6 des cônes conjuguée au matériau biocompatible Tilastan – E11,12 crée les conditions idéales pour assurer un ancrage stable et durable ainsi que pour la régénération osseuse.
La structure tridimensionnelle TrabecuLink, avec sa taille de pores, sa porosité et sa profondeur structurelle, offre également une excellente base pour favoriser l'ostéoconduction et la microvascularisation, eu égard à la nécessité de couche protéinique (fibronectine – vitronectine – fibrinogène) recouvrant toute la structure.1,2 Les cônes TrabecuLink peuvent être associés à la gamme genou Endo-Model éprouvée de LINK, dans une grande variété de tailles et de versions. Le choix des tailles correspond aux dimensions des prothèses de genou à charnière.
Stabilité – en cas de fixation métaphysaire9,13
- Renforcement de la structure osseuse en cas de défects osseux fémoraux et tibiaux
- Stabilité primaire élevée, aussi bien pour le cône TrabecuLink que pour les composants prothétiques cimentés dans ce dernier
- Sans ciment côté os, pour la régénération osseuse
Élasticité – grâce aux axes de flexion intégrés dans la paroi métallique interne
- Compression mécanique favorisant la régénération osseuse5,6
- Axes de flexion pour une adaptation aux surfaces osseuses
- Excellent ajustement grâce à l'élasticité liée à la construction qui facilite également l'insertion des cônes fémoraux/tibiaux TrabecuLink
- Effet ressort facilitant le positionnement peropératoire
Adaptabilité – pour une large gamme de solutions7
- Combinaison possible avec tous les composants de la gamme genou Endo-Model de LINK
- Tailles correspondant aux tailles des prothèses de genou à charnière
- Possibilité de fabrication de modèles spécifiques aux patients
Protection – grâce à la paroi métallique interne
- Empêche la pénétration de ciment osseux dans la structure TrabecuLink
- Fixation cimentée fiable grâce à des « rainures » positionnées en conséquence (pratique pour la reprise)
Respect de l'environnement3,8
- Fabrication respectueuse des ressources naturelles, en alliage de titane éprouvé
TrabecuLink
Structure tridimensionnelle pour une apposition osseuse optimale
- Géométrie des pores (porosité : 70 %, taille des pores : 610 à 820 μm, profondeur de structure : 2 mm) assurant une excellente adhésion cellulaire1,2,4
Remplissage des pores
La séquence d'images montre le remplissage d'un pore de la structure TrabecuLink par du tissu dans des conditions de culture cellulaire in vitro. Les fibres vertes visibles correspondent à la fibronectine sécrétée par les fibroblastes humains et réorganisée continuellement sur une période de huit jours. La fibronectine est un composant de la matrice extracellulaire qui se forme à un stade précoce du processus de cicatrisation. Elle constitue une base pour l'intégration du collagène indispensable à la minéralisation des tissus et à la croissance osseuse dans la structure. Outre l'accumulation croissante de fibronectine au fil du temps, on observe une contraction nette de la matrice vers le centre du pore. Ce mécanisme de contraction, attribuable aux forces cellulaires agissant dans le tissu, accélère la vitesse à laquelle le pore se remplit de tissu par rapport à une croissance couche par couche (référence : Joly P et al., PLOS One 2013; https://journals.plos.org/plosone/article?id=10.1371/journal.pone.0073545). Institut Julius Wolff, Hôpital universitaire de la Charité de Berlin

Cônes fémoraux TrabecuLink
4 tailles et 3 versions
- XS, S, M, L
- À 3 zones (à gauche et à droite),
à 2 zones (neutre),
proximal (neutre)

Références bibliographiques (générales)
- Cecile M. Bidan, Krishna P. Kommareddy, Monika Rumpler, Philip Kollmannsberger, Yves J.M. Brechet, Peter Fratzl, John W.C. Dunlop. et al.; How Linear Tension Converts to Curvature: Geometric Control of Bone Tissue Growth; PLoS ONE 7(5): e36336. https://doi.org/10.1371/journal.pone.0036336 (2012)
- Pascal Joly, Georg N. Duda, Martin Schöne, Petra B. Welzel, Uwe Freudenberg, Carsten Werner, Ansgar Petersen, et al.; Geometry-Driven Cell Organization Determines Tissue Growth in Scaffold Pores: Consequences for Fibronectin Organization; PLoS ONE 8(9): e73545. doi.org/10.1371/journal.pone.0073545 (2013)
- Dr. Malte Drobe, Franziska Killiches; Vorkommen und Produktion mineralischer Rohstoffe – ein Ländervergleich; Bundesanstalt für Geowissenschaften und Rohstoffe Hannover; http://www.bgr.bund.de/DE/Themen/Min_rohstoffe/Downloads/studie_rohstoffwirtschaftliche_einordnung_2014.pdf?__blob=publicationFile&v=4 (2014)
- Steinemann SG; Compatibility of Titanium in Soft and Hard Tissue – The Ultimate is Osseointegration; Materials for Medical Engineering, WILEY-VCH, Volume 2, Page 199-203
- Gerald Küntscher; Praxis der Marknagelung; Friedrich-Karl Schattauer-Verlag (1962)
- R. Texhammer, C. Colton et al.; AO-Instrumente und Implantate (Technisches Handbuch); Springer Verlag, 2. Auflage, S.25 (2011)
- Gabriele Panegrossi, corresponding author Marco Ceretti, Matteo Papalia, Filippo Casella, Fabio Favetti, and Francesco Falez; Bone Loss Management in Total Knee Revision Surgery; Int Orthop. 2014 Feb; 38(2): 419–427; www.ncbi.nlm.nih.gov/pmc/articles/PMC3923937/ (2014)
- Conflict Minerals: MEPs Secure Mandatory Due Diligence for Importers; Press release - External/international trade − 22-11-2016 - 19:07; www.europarl.europa.eu/news/en/news-room/20161122IPR52536/conflict-minerals-meps-secure-mandatory-due-diligence-for-importers (2016)
- Henricson A, Linder L, Nilsson KG.; A Trabecular Metal Tibial Component in Total Knee Replacement in Patients Younger than 60 Years: a Two-year Radiostereophotogrammetric Analysis; J Bone Joint Surg Br. 2008;90:1585–1593. doi: 10.1302/0301-620X.90B12.20797 (2008)
- P. K . Sculco, M. P. Abdel, A. D. Hanssen, D. G. Lewallen; The Management of Bone Loss in Revision Total Knee Arthroplasty; Bone Joint J 2016;98-B(1 Suppl A):120–4 (2016)
- Peter Heinl, Lenka Müller, Carolin Körnera, Robert F. Singera, Frank A. Müllerb; Cellular Ti–6Al–4V Structures with interconnected Macro Porosity for Bone Implants Fabricated by Selective Electron Beam Melting; Acta Biomaterialia Volume 4, Issue 5, September 2008, Pages 1536–1544 (2008)
- Hong Wang, Bingjing Zhao, Changkui Liu, Chao Wang, Xinying Tan, Min Hu; A Comparison of Biocompatibility of a Titanium Alloy Fabricated by Electron Beam; PLOS ONE | DOI:10.1371/journal.pone.0158513 July 8 2016, (2016)
- Ivan De Martino, Vincenzo De Santis, Peter K Sculco, Rocco D’Apolito, Joseph B Assini, Giorgio Gasparini; Tantalum Cones Provide Durable Mid-Term Fixation in Revision TKA; Clin Orthop Relat Res 473 (10), 3176-3182 (2015)